
LENGKAP ‼️ Cara Mudah Menentukan Pasangan Asam Basa Konjugasi TeoriAsamBasa AsamBasaKonjugasi
Ba (OH)2 adalah senyawa yang mudah larut dalam air, sehingga reaksi ionisasi Ba (OH)2 diwakili oleh persamaan berikut: Ba (OH)2 → Ba2+ + 2 OH-. Dalam reaksi ini, satu molekul Ba (OH)2 terurai menjadi satu ion barium (Ba2+) dan dua ion hidroksida (OH-). Ion-ion ini memiliki muatan listrik yang berbeda dan membentuk ikatan ionik yang kuat.

Asam Basa Teori, Contoh, dan Sifat Asam Basa InformasainsEdu
Barium hidroksida mengalami dekomposisi hingga menjadi barium oksida pada saat dipanaskan mencapai suhu hingga 800 °C. Reaksi dengan karbondioksida dapat menghasilkan barium karbonat. Senyawa ini bertindak seperti basa, sehingga pada saat direaksikan dengan asam maka akan mengalami reaksi netralisasi.

7. Tentukan persamaan kimia berikut magnesium hidroksida + asam asetat Mylanta
Pembahasan Menurut Arrhenius, basa didefinisikan sebagai zat yang jika dilarutkan dalam air maka dapat menghasilkan ion OH − . Senyawa barium hidroksida memiliki rumus molekul Ba ( OH ) 2 , ketika dilarutkan dalam air menghasilkan OH − , sesuai persamaan reaksi berikut: Ba ( OH ) 2 ( s ) → Ba 2 + ( aq ) + 2 OH − ( aq ) Dengan demikian, maka jawaban yang tepat adalah sesuai penjelasan.

Teori Asam Basa
Barium adalah unsur kelima pada golongan 2 dan merupakan logam alkali tanah yang lunak dan keperakan. Barium tidak pernah ditemukan di alam sebagai unsur bebas karena reaktivitas kimianya yang tinggi. Hidroksidanya, yang dikenal dalam sejarah pra-modern sebagai barita, tidak terjadi sebagai mineral, tetapi dapat dibuat dengan memanaskan barium.
Teori Asam Basa dan Garam Siswapedia
Materi Asam, Basa, Garam : Pengertian, Sifat, Ciri, Macam & Contohnya [LENGKAP] - Asam adalah zat yang dalam air dapat menghasilkan ion hidrogen (H+).. Barium Hidroksida (Ba(OH)2) 2. Basa Lemah.. barium klorida bersifat asam atau basa, barium sulfat asam atau basa, Basa, basa adalah, berapakah ph asam dan basa, beri 3 contoh garam netral,.

PPT TEORI ASAM DAN BASA PowerPoint Presentation, free download ID3560268
Basa kuat adalah adam love Valen sederhana yang dapat mendeprotonasi asam sangat lemah di dalam reaksi asam-basa. Contoh paling umum dari basa kuat adalah hidroksida dari logam alkali dan logam alkali tanah seperti NaOH dan Ca(OH) 2. Berikut ini adalah daftar basa kuat: Kalium hidroksida (KOH) Barium hidroksida (Ba(OH) 2) Cesium hidroksida (CsOH)

Cara Menentukan Senyawa Bersifat Asam Basa Atau Netral Digunakan
Bagaimana menentukan kuat atau lemahnya asam/basa berdasar nilai tetapan kesetimbangannya masing-masing? Dalam jurnal kimia internasional ini pernah dibahas tentang batas nilai Ka suatu asam lemah-asam kuat. Jika nilai Ka suatu asam > 0,1 maka suatu asam dapat dikategorikan sebagai asam kuat.. Barium hidroksida: Ba(OH) 2 *

Pengertian Asam dan Basa Serta Penggunaannya
Barium hidroksida mengalami dekomposisi menjadi barium oksida saat dipanaskan hingga mencapai suhu 800 °C. Reaksi dengan karbon dioksida akan menghasilkan barium karbonat. Senyawa ini bertindak seperti basa, sehingga jika direaksikan dengan asam akan mengalami reaksi netralisasi. Maka dari itu, senyawa ini akan membentuk barium sulfat jika.

Mg Oh 2 Basa Kuat Atau Lemah cara bertanya yang baik kepada guru
10 Sifat Basa beserta Contohnya. pH lebih dari 7,0. Basa terasa licin. Berbentuk padat kecuali amonia yang merupakan gas. Memiliki rasa pahit. Kekuatan bergantung pada konsentrasi ion hidroksida. Elektrolit, menghantarkan listrik. Menghasilkan ion OH - dalam air. Rumus kimia basa diakhiri dengan OH.

Contoh Soal menentukan pasangan asam basa konjugasi menurut BronstedLowry YouTube
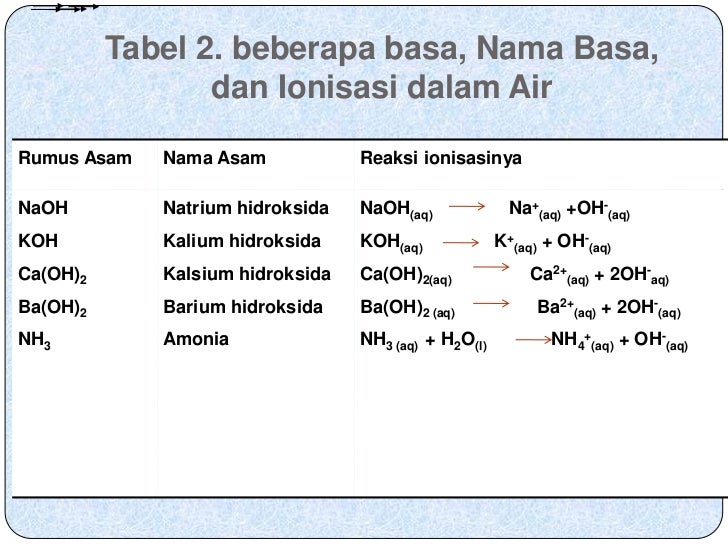
Suatu larutan dapat diketahui apakah sifatnya asam atau basa saat berada dalam bentuk larutan. Ada tiga teori asam basa yang sangat dikenal yakni oleh Arrhenius, Brønsted-Lowry, dan Lewis.. nalium hidroksida, kalsium hidroksida, dan barium hidroksida. Natrium hidroksida. NaOH(aq)\rarr Na^+(aq)+OH^-(aq) Kalium hidroksida.
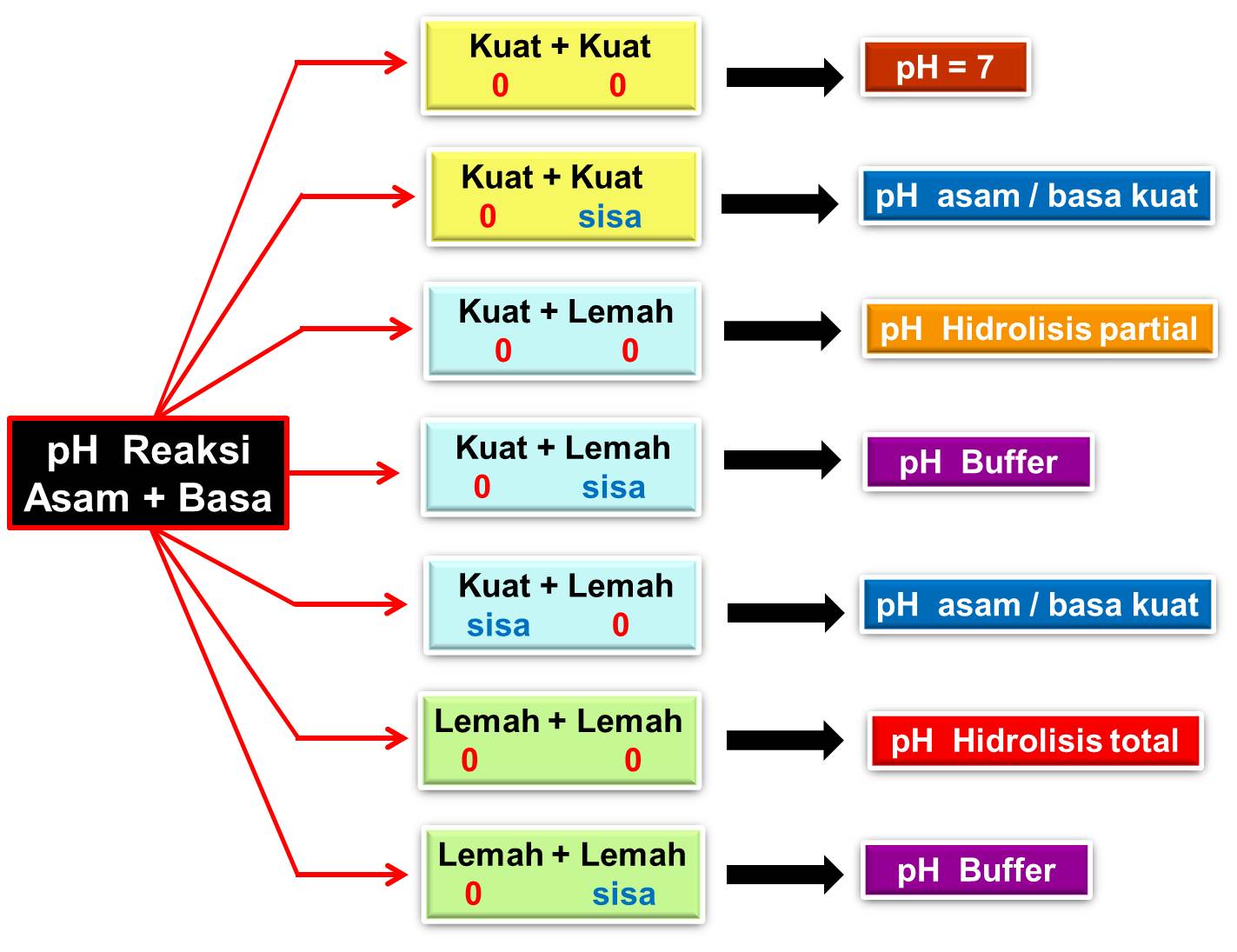
CINTA KIMIA PH REAKSI ASAM DAN BASA
Contoh dari basa kuat seperti natrium hidroksida (NaOH), litium hidroksida (LiOH), kalium hidroksida (KOH), barium hidroksida (Ba(OH)2), dan kalsium hidroksida (Ca(OH)2). 2. Asam lemah dan basa lemah. Asam lemah adalah asam yang hanya terionisasi sebagian di dalam air sehingga nilai a-nya kecil.

Uji Asam Basa Menggunakan Indikator Alami Praktikum Kimia Kelas 11 MIPA YouTube
Sementara basa adalah zat yang menghasilkan ion hidroksida (OH-) dalam larutan. Asam dan basa dapat bereaksi menghasilkan air serta senyawa ionic garam. Reaksi itu disebut reaksi netralisasi. Asam dan basa merupakan dua jenis larutan yang kerap digunakan dalam kehidupan sehari-hari manusia. Asam dan basa ada yang memiliki sifat kuat dan juga lemah.

LENGKAP ‼️ REAKSI ASAM BASA KELAS 11 ‼️ REAKSI PENGGARAMAN YouTube
Sementara basa kuat adalah senyawa basa yang jika dilarutkan dalam air mudah melepaskan ion OH-, larutan basa ini juga akan mengalami disosiasi total. Contoh basa kuat misalnya kalium hidroksida (KOH), natrium hidroksida atau sodium hidroksida (NaOH), dan barium hidroksida (Ba(OH)2). 2. Asam Lemah dan Basa Lemah

Mengenal Asam Basa Sifat, Cara Membedakan, dan Klasifikasinya Kimia Kelas 11
Asam atau Basa? Barium hidroksida adalah basa kuat. Ini berarti bahwa ketika senyawa ini bereaksi dengan air, ia akan melepaskan ion hidroksida (OH-) ke dalam larutan, membuatnya basa. Sebagai contoh, ketika Ba (OH)2 dilarutkan dalam air, itu akan menghasilkan larutan basa dengan pH tinggi.
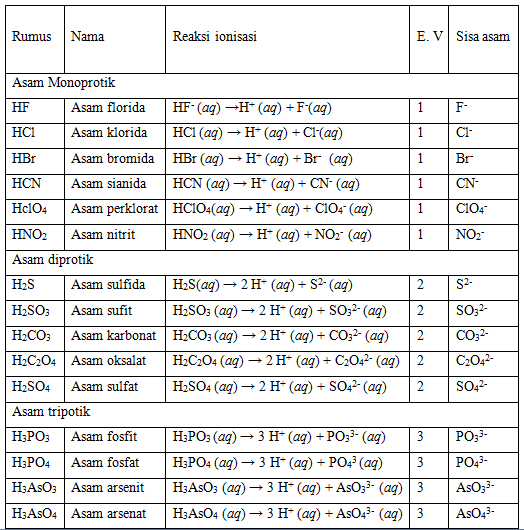
Reaksi Ionisasi Asam Basa
Kalau pada suhu 25℃, pH < 7 bersifat asam, pH = 7 bersifat netral, dan pH > 7 bersifat basa. Derajat keasaman dan kebasaan suatu larutan. (dok. Flickr/boellstiftung) Semakin kecil nilainya, maka larutan tersebut akan semakin asam. Misalnya antara larutan dengan pH 3 dan 1, akan lebih kuat konsentrasi asam dengan pH 1 daripada 3.
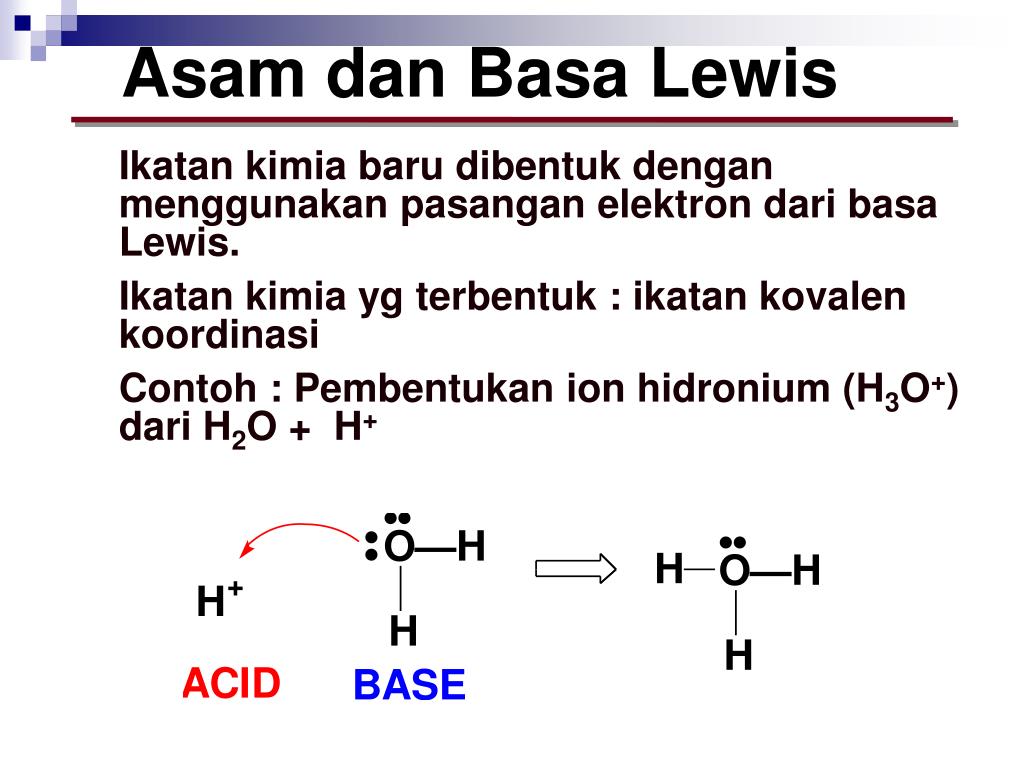
PPT ASAM DAN BASA PowerPoint Presentation, free download ID1244635
HNO3 : Asam Nitrat; H3PO4 : Asam Fosfat; Tata Nama Senyawa Basa Senyawa basa adalah senyawa ion yang terdiri dari kation logam dan anion OH -. Nama senyawa basa sama dengan nama kationnya yang diikuti kata hidroksida. Contoh rumus senyawa basa: Al(OH)3 : Aluminium Hidroksida; Ba(OH)2 : Barium Hidroksida; Cu(OH)2 : Tembaga(II) Hidroksida.